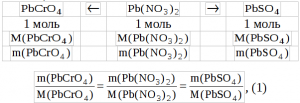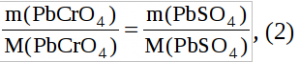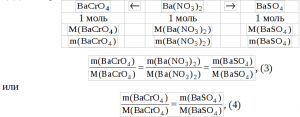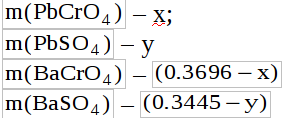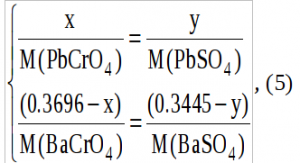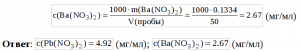Химия. 11 класс
Задание 1. Для полного гидролиза смеси двух сложных эфиров потребовалось 40 г 14%-ного раствора гидроксида калия. При добавлении к такому же количеству смеси избытка аммиачного раствора оксида серебра выделилось 8,64 г осадка. Определите строение сложных эфиров и их содержание в исходной смеси в мольных процентах.
Решение:
Запишем уравнения щелочного гидролиза эфиров:
RCOOR1 + KOH = RCOOK + R1OH
R2COOR3 + KOH = R2COOK + R3OH
В реакцию вступило 40∙0,14/56 = 0,1 моль КОН, следовательно, общее количество сложных эфиров в смеси тоже равно 0,1 моль, а средняя молярная масса этой смеси равна Мср = 6,84/0,1 = 68,4 г/моль. Это означает, что молярная масса одного из этих эфиров больше 68,4 г/моль, а другого – меньше этой величины.
Из всех сложных эфиров самый легкий – метилформиат H-CO-O-CH3 (М = 60 г/моль). Все остальные эфиры имеют молярную массу больше 68,4 г/моль. Таким образом, один из двух эфиров – метилформиат. Его количество можно определить по реакции серебряного зеркала. При окислении альдегидной группы метилформиата образуется метиловый эфир угольной кислоты H-CO-O-CH3, который гидролизуется в аммиачном растворе с образованием метилового спирта и гидрокарбоната аммония:
HCOOCH3 + 2[Ag(NH3)2]OH = CH3OH + 2Ag + NH4HCO3 + 3 NH3
По этому уравнению n(HCOOCH3) = n(Ag)/2 = (8,64/108)/2 = 0,04 моль (40% мольных).
m(HCOOCH3) = 0,04∙60 = 2,4 г.
Масса второго эфира равна 6,84 – 2,4 = 4,44 г, а его количество составляет 0,1 – 0,04 = 0,06 моль, следовательно молярная масса равна М (R2COOR3) = 4,44/0,06 = 74 г/моль. Только два эфира имеют такую молярную массу: HCOOC2H5 и СH3COOCH3. Но второй эфир не может быть эфиром муравьиной кислоты, поскольку тогда по реакции серебряного зеркала выделилось бы больше серебра (0,2 моль вместо 0,08 моль). Следовательно, второй эфир – метилацетат СH3COOCH3 (n = 0.06 моль, или 60% мольных в смеси).
Ответ: метилацетат СH3COOCH3 (60% мольных в смеси), метилформиат (40% мольных в смеси)
Задание 2. Простое желтое вещество А при нагревании взаимодействует с бесцветным газом Б, который можно получить при разложении бертолетовой соли, образуя газ В, обладающий резким запахом. При пропускании газа В через раствор гидроксида натрия образуется соль Г, которую применяют в фотографии. Газы Б и В реагируют при нагревании над катализатором V2O5, образуя вещество Д. Это вещество, растворяясь в воде, дает кислоту Е, которая с раствором BaCl2 образует белый нерастворимый в воде осадок. При действии кислоты Е на соль Г выделяется газ В. Назовите вещества А, Б, В, Г, Д и Е. Напишите уравнения соответствующих реакций. Какой максимальный объем газа В может быть поглощен 500 мл 10%-ного раствора гидроксида натрия?
Решение:
Простое желтое вещество А – сера, бесцветный газ Б – кислород:
2KClO3 → 2KCl + 3O2 (катализатор MnO2). (1)
Газ В – SO2
S + O2 → SO2. (2)
При взаимодействии SO2 с раствором NaOH возможно образование двух типов солей: NaHSO3 (соль Г) и Na2SO3:
SO2 + NaOH → NaHSO3, (3)
1 моль (22,4 л) 1 моль (40 г)
х л 55,5 г
SO2 + 2NaOH → Na2SO3 + Н2О. (4)
1 моль 2 моля
Вещество Д – SO3:
2SO2 + O2 → SO3, (катализатор V2O5). (5)
Кислота Е – H2SO4:
SO3 + H2O → H2SO4, (6)
H2SO4 + BaCl2 → BaSO4 + 2 HCl, (7)
2NaHSO3 + H2SO4 → Na2SO4 + 2SO2 + 2 H2O. (8)
Максимальный объем SO2 поглощается щелочью в соответствии с уравнением реакции (3). Масса раствора NaOH равна 555 г(500 (мл)*1,11 (г/мл)).
100 г 10%-ного раствора щелочи содержат — 10 г NaOH;
555 г 10%-ного раствора щелочи содержат — х г NaOH,
отсюда х = 55,5 г NaOH.
Максимальный объем газа SO2, поглощаемый раствором NaOH, по уравнению (3) равен:
[55,5 (г) * 22,4 (л)].40 (г) = 31,08 л.
Ответ: А – сера; Б – кислород; В – оксид серы (IV); Г – гидросульфит натрия; Д — оксид серы (VI); Е – серная кислота; объем SO2 равен 31,08 л.
Задание 3. Вычислите процентную концентрацию раствора, образовавшегося в результате электролиза на платиновых электродах 500 мл 20%-ного раствора хлората натрия (p=1,15 г/см3), если известно, что через раствор был пропущен ток, силой 5 А в течение 1 часа (катодное и анодное пространство не разделены).
Решение:
Составим уравнение полуреакций, протекающих на электродах при электролизе водного раствора NaClO3:
На катоде (-): 2Н2О + 2е → Н2↑ + 2ОН—.
На аноде (+): 2Н2О – 4е → О2 + 4H+.
У анода атомарный кислород в момент выделения может окислить хлорат-ион (ClO3—) до перхлорат-иона (ClO4—): ClO3— + O → ClO4—.
У катода выделяется водород и в катодном пространстве накапливается щелочь, в анодном – хлорная кислота. Если катод и анод не разделены, то в результате электролиза раствора хлората натрия получается перхлорат натрия. Таким образом, суммарное уравнение электролиза имеет вид:
NaClO3 + H2O → NaClO4 + H2↑.
Количество выделившегося Н2 можно определить, воспользовавшись законом Фарадея:
m(H2) = (M*I*t)/z*F,
F – число Фарадея (96485 Кл/моль), M – молекулярная масса водорода (г/моль), I – сила тока (в амперах), t – время (в секундах), z – число электронов, принятых (или отданных) в окислительно-восстановительном процессе. После подстановки, получаем:
m(H2) = (2 (г/моль)*5 (А)*3600 (с))/2*96485 (Кл/моль) = 0,1866 г.
Первоначальная масса раствора 500 (см3) * 1,15 (г/см3) = 575 г в результате электролиза уменьшилась на 0,1866 г и составила 574,81 г.
Масса вступившего в реакцию NaClO3 составила 9,9365 г. Масса образовавшегося NaClO4 составила 11,4293 г. Таким образом, масса растворенных веществ в растворе после электролиза составила: 575 (г) 0,2 – 9,9365 (г) + 11,4293 (г) = 116,4928 г.
В итоге, процентная концентрация получившегося раствора составляет:
ω= (116,4928 (г)/574,81 (г))*100% = 20,27 %
Ответ: ω=20,27 %.
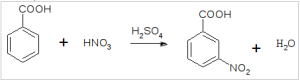
Задание 4. Предложите схему получения 3-нитробензойной кислоты из кумола (изопропилбензола). Укажите условия реакций.
Решение:
Изопропильная группа – ориентант 1-ого рода, поэтому при нитровании кумола будет образовываться смесь пара— и орто-изомеров с преобладанием первого (по пространственным причинам). Поэтому для введения нитрогруппы в мета-положение необходимо провести окисление изопропильной группы до карбоксильной, которая, будучи ориентантом 2-ого рода, будет направлять последующую электрофильную атаку в мета-положение.
1 стадия – окисление кумола в бензойную кислоту, например, KMnO4 в кислой среде при нагревании: ![]()
2 стадия – нитрование бензойной кислоты смесью конц. HNO3 и H2SO4 или конц. H2SO4 и NaNO3:
Задание 5. К 30 л смеси, состоящей из аргона и этиламина, добавили 20 л бромоводорода, после чего плотность газовой смеси по воздуху стала равна 1,814. Вычислите объемные доли газов в исходной смеси.
Решение:
При реакции газообразных веществ образуется твердое вещество, которое уходит из сферы реакции:
C2H5NH2 + HBr = [C2H5NH3]Br
Пусть в исходной смеси содержалось х л аргона и у л этиламина. Тогда х + у = 30.
Средняя молярная масса газовой смеси после реакции равна Мср = 1,814∙29 = 52,6 г/моль. Это означает, что в газовой смеси находятся аргон и бромоводород (если бы в смеси остались аргон (М = 40) и этиламин (М = 45), то 40 < Мср < 45). Объем аргона остался неизменным V(Ar) = x л, а исходный объем HBr уменьшился за счет реакции на у л: V(HBr) = (20 – у) л. Теперь используем выражение средней молярной массы через объемы газов:
Мср = (M1V1 + M2V2)/(V1+V2) = (40x + 81(20 – y))/(x + 20 — y) = 52,6
V = x + y = 30
Решая систему уравнений, находим:
х = 18 л – V (Ar)
y = 12 л – V (C2H5NH2).
Объемная доля аргона (18/30) 100 = 60%, объемная доля этиламина 40%.
Ответ: ω(C2H5NH2)=40% (по объему), ω(Ar)=60% (по объему)
Задание 6. Из исследуемого раствора, содержащего Ba(NO3)2 и Pb(NO3)2, отобрали две пробы по 50.00 мл каждая. К первой пробе добавили избыток раствора (NH4)2CrO4, а ко второй избыток разбавленной H2SO4. Масса выпавшего осадка в первой пробе составила 0.3696 г, а во второй – 0.3445 г. Рассчитайте концентрацию и в мг/мл в исследуемом растворе.
Решение: При добавлении к 1-ой пробе избытка (NH4)2CrO4 образуется осадок, состоящий из BaCrO4 и PbCrO4: ![]()
При добавлении к 2-ой пробе разбавленной H2SO4 образуются осадки BaSO4 и PbSO4:
На основании представленных уравнений реакций и мольных соотношений реагирующих веществ можно записать:
1) Для нитрата свинца
или
Объединим уравнения (2) и (4) в систему уравнений введя предложенные обозначения:
Решая систему (5), получаем:
x= 0.2403 (m(PbCrO4))
y=0.2254 (m(PbSO4))
Соответственно m(BaCrO4) и m(BaSO4) равны: ![]()
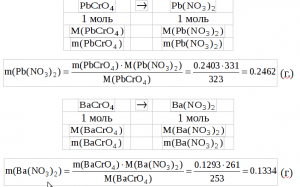
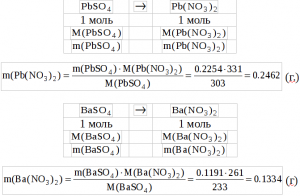
Затем определяем m(Pb(NO3)2) и m(Ba(NO3)2
Зная массы нитратов бария и свинца, находим их концентрацию (мг/мл): ![]()